ГОСТ 31214-2016
Изделия медицинские. Требования к образцам и документации, представляемым на токсикологические, санитарно-химические исследования, испытания на стерильность и пирогенность
Купить ГОСТ 31214-2016 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает требования к документации и образцам медицинских изделий и материалов, представляемым на оценку биологической безопасности, включающей токсикологические, санитарно-химические исследования, испытания на стерильность и пирогенность.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Общие положения об организации Исследований медицинских изделий и материалов
5 Требования к документации и образцам, представляемым на Исследования
6 Оформление результатов Исследований
Приложение А (обязательное) Форма и количество представляемых образцов медицинских изделий, материалов
| Дата введения | 01.10.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 31.08.2016 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 90-П |
|---|---|---|---|
| 21.10.2016 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1483-ст |
| Разработан | ООО НТЦ МЕДИТЭКС | ||
| Издан | Стандартинформ | 2016 г. |
Medical devices. Requirements for samples and documentation presented for toxicological tests, sanitary and chemical analyses, tests for sterility and pyrogenicity
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7
стр. 8
стр. 9

стр. 10

стр. 11
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ. МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION. METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ
Требования к образцам и документации, представляемым на токсикологические, санитарно-химические исследования, испытания на стерильность и пирогенность
ГОСТ
31214-
2016
Издание официальное
|
Москва Стандартинформ 2016 |
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Обществом с ограниченной ответственностью «Научно-технический центр «МЕДИТЭКС» (ООО «НТЦ «МЕДИТЭКС»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 31 августа 2016 г. №90-П)
|
За принятие проголосовали: | ||||||||||||||||||
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 21 октября 2016 г. № 1483-ст межгосударственный стандарт ГОСТ 31214-2016 введен в действие в качестве национального стандарта Российской Федерации с 1 октября 2017 г.
5 ВЗАМЕН ГОСТ 31214-2003
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ. 2016
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Редактор А.В Хрусталев Технический редактор В Н. Прусакова Корректор И А Королева Компьютерная верстка И.А. Налоикиной
Сдано в набор 26 102016 Подписано в печать 02 11 2016 Формат 60*84* Гарнитура Ариал Уел. печ. л. 1.40 Уч -изд л. 1.27. Тираж 25 это Зак. 2711.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Издано и отпечатано во ФГУП «СТАНДАРТИНФОРМ». 123995 Москва. Гранатный пер 4 www.gos6nfo.ru info@gosbnfo ru
Содержание
1 Область применения...................................................1
2 Нормативные ссылки..................................................1
3 Термины и определения................................................1
4 Общие положения об организации Исследований медицинских изделий и материалов.........2
5 Требования к документации и образцам, представляемым на Исследования...............2
6 Оформление результатов Исследований......................................3
Приложение А (обязательное) Форма и количество представляемых образцов медицинских изделий.
материалов................................................5
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ
Требования к образцам и документации, представляемым на токсикологические, санитарно-химические исследования, испытания на стерильность и лирогенность
Medical devices. Requirements for samples and documentation presented for toxicological tests, sanitary and chemical
analyses, tests for sterility and pyrogenicity
Дата введения — 2017—10—01
1 Область применения
Настоящий стандарт устанавливает требования к документации и образцам медицинских изделий и материалов, представляемым на оценку биологической безопасности, включающей токсикологические, санитарно-химические исследования, испытания на стерильность и лирогенность (далее — Исследования).
Стандарт не распространяется на документацию и образцы медицинских изделий, изготовленных по индивидуальным заказам пациентов, к которым предъявляются специальные требования по назначению медицинских работников и которые предназначены исключительно для личного использования конкретным пациентом.
2 Нормативные ссылки
В настоящем стандарте использована нормативная ссылка на следующий межгосударственный стандарт:
ГОСТ 31576-2012 Оценка биологического действия медицинских стоматологических материалов и изделий. Классификация и приготовление проб
Примечание — При пользооании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (изменяющим) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 медицинские изделия: Любые инструменты, аппараты, приборы, оборудование, материалы и прочие изделия, применяемые в медицинских целях отдельно или в сочетании между собой, а также вместе с другими принадлежностями, необходимыми для применения указанных изделий по назначению. включая специальное программное обеспечение, и предназначенные производителем для профилактики. диагностики, лечения и медицинской реабилитации заболеваний, мониторинга состояния организма человека, проведения медицинских исследований, восстановления, замещения, изменения анатомической структуры или физиологических функций организма, предотвращения или прерывания
Издание официальное
беременности, функциональное назначение которых не реализуется путем фармакологического, иммунологического, генетического или метаболического воздействия на организм человека.
Примечание — Изделие, е состав которого входит лекарственное средство, относится к медицинским изделиям, если лекарственное средство выполняет вспомогательную функцию.
3.2 материал: Любой синтетический или природный полимер, металл, сплав, керамика, композиты или другой нежизнеспособный материал, включая нежизнеспособную биологическую ткань, продукты биоинженерии, применяемые в качестве медицинского изделия или его части.
3.3 токсикологические исследования: Исследования, проводимые с целью выявления токсического действия изделий и материалов на биологические объекты.
3.4 санитарно-химические исследования: Исследования, проводимые с целью определения опасных химических веществ, мигрирующих в модельную среду из медицинского изделия или материала.
3.5 испытания на стерильность: Испытания медицинского изделия на наличие жизнеспособных микроорганизмов.
3.6 испытания на пирогенностъ: Испытания медицинского изделия на наличие веществ, вызывающих повышение температуры тела.
4 Общие положения об организации Исследований медицинских изделий и материалов
4.1 Исследования медицинского изделия проводят в организациях, аккредитованных на данный вид деятельности в соответствии с действующим законодательством и имеющих соответствующую область аккредитации.
Исследования медицинских изделий и материалов проводят:
- в целях государственной регистрации:
- по инициативе изготовителя/заявителя;
- в целях подтверждения соответствия.
4.2 Программу Исследований медицинского изделия или материала составляют специалисты, проводящие Исследования; программа определяется видом и длительностью контакта изделия с организмом человека, химической природой материалов, технологией изготовления, способом стерилизации изделия. Программа является неотъемлемой частью заключения/протокола и оформляется в виде приложения.
4.3 Исследования проводят в соответствии с требованиями действующих нормативных документов.
4.4 Исследования необходимо также проводить в случае изменения материалов медицинского изделия, технологии изготовления, метода стерилизации, упаковки, назначения медицинского изделия.
5 Требования к документации и образцам, представляемым на Исследования
Для проведения Исследований медицинского изделия должны быть представлены:
- справка об изделии (пояснительная записка);
- техническая документация;
- сведения о нормативной документации;
- руководство по эксплуатации/инструкция по применению;
- образцы медицинского изделия.
Для проведения Исследований медицинского изделия иностранного производства информацию об изделии и документацию представляют на русском языке, заверенную в установленном порядке.
5.1 Комплект документов должен содержать следующую информацию:
- информацию об изготовителе, месте производства;
- информацию о заявителе;
- наименование медицинского изделия в соответствии с технической документацией:
- назначение медицинского изделия с указанием сферы применения (в том числе и принадлежностей);
2
- вид контакта медицинского изделия с организмом человека, длительность контакта и кратность применения (если изделие сложное, вид контакта должен быть указан для каждой детали, узла и для принадлежностей);
- для имплантируемых изделий, клеев, сорбентов и гемостатических материалов указывают максимальное количество применяемого медицинского изделия за одну процедуру;
- класс потенциального риска применения медицинского изделия;
- перечень принадлежностей;
- комплектность поставки;
- материалы, из которых изготовлено медицинское изделие и принадлежности (для сложных изделий указывают материалы для деталей, узлов и других составляющих), с указанием марок;
- сертификат/паслорт на материалы (при наличии);
- информацию о первичной упаковке с указанием нормативных документов и материалов упаковки;
- информацию о стерильности/нестерильности, способе стерилизации медицинского изделия и принадлежностей к нему в соответствии с технической документацией, а также информация о способе стерилизации медицинских изделий, поставляемых в нестерильном виде, но применяемых стерильными;
- наименование и номер фармакопейной статьи (или ее копия) на лекарственные средства в случае применения их в составе медицинского изделия.
Организация, проводящая Исследования, вправе запросить и другую информацию, необходимую для их проведения.
Представляемая документация должна сопровождаться описью в двух экземплярах.
5.2 Требования к образцам
5.2.1 Медицинское изделие, применяемое в стерильном виде, но поставляемое не стерильным, должно быть представлено на Исследования в двух вариантах: нестерильным и подвергнутым стерилизации в соответствии с технической документацией изготовителя.
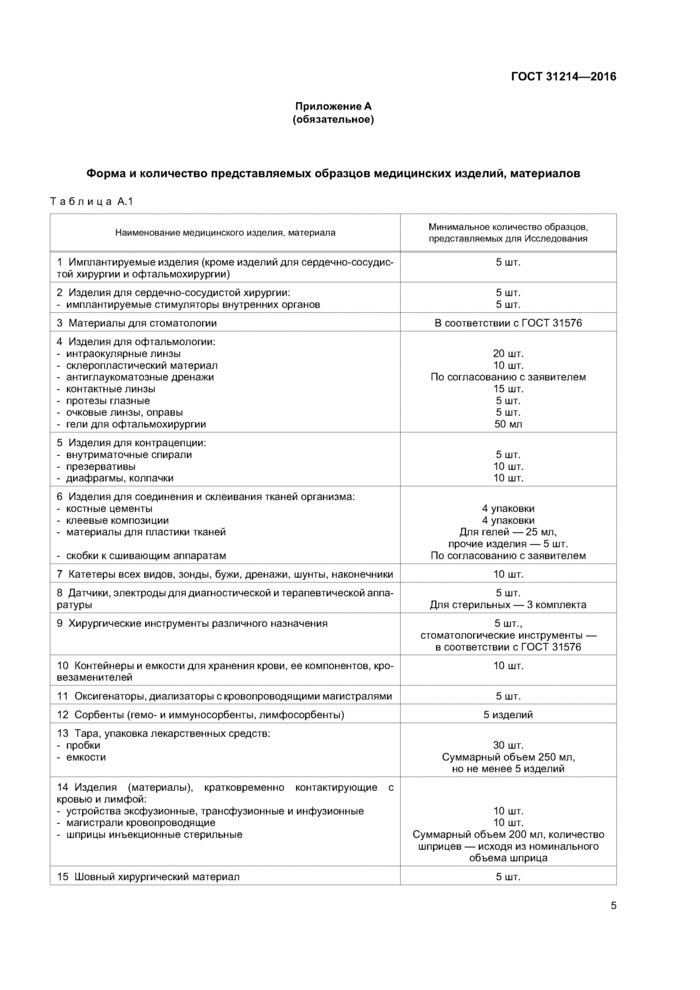
5.2.2 Образцы изделий представляют на Исследования в количестве, указанном в таблице А.1 приложения А. Изделия, не вошедшие в указанную таблицу, представляют на Исследования в количестве, согласованном с организацией, проводящей Исследования.
5.2.3 Образцы представляют в виде готового к обращению медицинского изделия, упакованного и маркированного в соответствии с технической документацией.
Для материалов отечественного и иностранного производства, предполагаемых к применению в медицинских изделиях (на этапе, предшествующем разработке изделия), форма и количество представляемых образцов оговаривается в каждом конкретном случае.
6 Оформление результатов Исследований
6.1 На основании анализа документации и проведенных Исследований оформляют заключе-ние/протокол.
6.2 В заключении/протоколе должны содержаться следующие сведения:
- информация об организации, проводящей Исследования (полное наименование, адрес, телефон и др );
- номер аттестата аккредитации, дата его выдачи, срок действия:
- наименование медицинского изделия согласно технической документации;
- информация о заявителе;
- адрес места изготовления;
- цель проведения Исследований;
- основание для проведения Исследований;
- перечень представленных документов;
- назначение медицинского изделия;
- вид и длительность контакта медицинского изделия с организмом человека;
- класс потенциального риска применения медицинского изделия;
- информация о стерильности/нестерильности. способе стерилизации и кратности применения. Для медицинского изделия, применяемого в стерильном виде, но поставляемого не стерильным, указывают способ стерилизации и кратность применения в соответствии с технической документацией производителя:
- сведения о применяемых материалах, составе;
3
- сведения об упаковке;
- перечень нормативных документов, на соответствие требованиям которых проведены Исследования;
- программа Исследований с указанием методов, применяемых средств измерений, испытательного и вспомогательного оборудования;
- изложение результатов Исследований;
- выводы о соответствии (несоответствии) требованиям нормативной документации, о биологической безопасности медицинского изделия.
4
Приложение А (обязательное)
Форма и количество представляемых образцов медицинских изделий, материалов
| ||||||||||||||||||||||||||||||||||
|
5 |
|
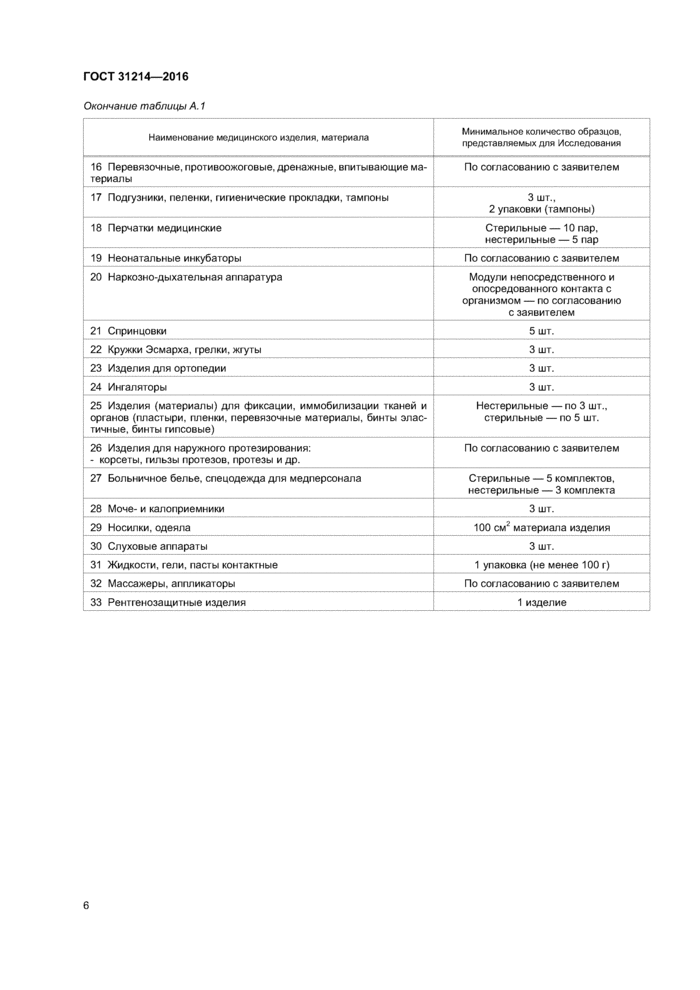
Окончание таблицы А. 1 | ||||||||||||||||||||||||||||||||||||||
|
6
УДК 615.46:002:006.354 МКС 11.040.01 ОКП944000
Ключевые слова: документация, образцы медицинских изделий, исследования токсикологические, исследования санитарно-химические, испытания на стерильность и лирогенность
7